Những đặc trưng nào, ngoài khối lượng nguyên tử, có thể làm cơ sở để phân loại các nguyên tố hóa học?
Cùng một nguyên tố có thể có những tính chất vật lí rất khác nhau tùy thuộc vào dạng đơn chất mà nó tạo thành. Tuy nhiên, khi xét đến tính chất hóa học – yếu tố quyết định khả năng phản ứng của các chất – thì vấn đề trở nên phức tạp hơn nhiều. Vì vậy, mọi nỗ lực phân loại các nguyên tố dựa trên tính chất hóa học của các chất do chúng tạo thành đều không thành công. Do đó, cần phải đưa vào cơ sở phân loại một đặc trưng chung của tất cả các nguyên tố, chẳng hạn như khối lượng tương đối của nguyên tử.
1. Cách sắp xếp các nguyên tố trước Mendeleev
Tại sao hầu hết các nỗ lực sắp xếp các nguyên tố hóa học đều xuất hiện vào giữa thế kỉ XIX?
Nhiều nhà hóa học đã cố gắng tìm ra mối liên hệ giữa tính chất hóa học và khối lượng nguyên tử của các nguyên tố đã được phát hiện trước đó cũng như những nguyên tố mới được tìm ra.
Năm 1817, khi phân loại các nguyên tố kiềm thổ (canxi – stronti – bari) vào một nhóm riêng biệt, nhà hóa học người Đức Johann Wolfgang Döbereiner nhận thấy rằng khối lượng nguyên tử của nguyên tố ở giữa trong ba nguyên tố có tính chất vật lí và hóa học tương tự nhau xấp xỉ bằng trung bình cộng khối lượng nguyên tử của hai nguyên tố còn lại. Sau đó, ông phát hiện thêm các bộ ba nguyên tố có tính chất tương tự như lithium – natri – kali; lưu huỳnh – selen – telu; clo – brom – iốt. Ông gọi các nhóm này là “nhóm tam tố”. Vào thời điểm đó, khối lượng nguyên tử của brom trong nhóm tam tố cuối cùng vẫn chưa được xác định. Döbereiner đã tính khối lượng nguyên tử của brom theo quy tắc của mình: nếu khối lượng nguyên tử của clo và iốt lần lượt là 35,5 và 127 thì khối lượng nguyên tử của brom phải là (35,5 + 127) / 2 = 81,2, gần đúng với giá trị thực nghiệm.
Năm 1849, nhà hóa học người Nga Germain Henri Hess đã sắp xếp các nguyên tố phi kim có tính chất hóa học tương tự thành bốn nhóm: cacbon – bo – silic; nitơ – phốt pho – asen; lưu huỳnh – selen – telu; clo – brom – iốt. Hess không quá coi trọng hệ thống phân loại của mình, dù đã trình bày trong cuốn sách “Cơ sở của hóa học cơ bản”. Ông cho rằng hệ thống này còn chưa hoàn chỉnh, nhưng ít nhất đã giúp tập hợp các nguyên tố có tính chất giống nhau vào cùng một nhóm. Hess được xem là người đầu tiên đưa ra khái niệm “nhóm nguyên tố”. Tuy nhiên, sau này người ta nhận ra rằng bo không thuộc nhóm cacbon mà thuộc nhóm cùng với nhôm, indi và tali; sau đó gali cũng được bổ sung vào nhóm này.
Năm 1857, nhà hóa học người Anh William Odling công bố bảng các nguyên tố hóa học đầu tiên của mình. Sau đó, ông tiếp tục xây dựng các bảng khác, bao gồm 57 nguyên tố được chia thành bảy nhóm và sắp xếp theo thứ tự tăng dần của khối lượng nguyên tử. Các bảng này dựa trên sự tương đồng về tính chất hóa học của các nguyên tố. Những vị trí của các nguyên tố chưa biết được ông kí hiệu bằng dấu “–”. Bảng cuối cùng của Odling được công bố năm 1868. Tuy nhiên, ông không khẳng định mình là người đầu tiên phát hiện ra định luật tuần hoàn.
Một trong những nỗ lực đáng chú ý khác là “đường xoắn ốc” của nhà khoa học Pháp Alexandre-Emile Béguyer de Chancourtois. Năm 1862, ông đề xuất một hệ thống phân loại theo mô hình không gian, trong đó các nguyên tố được sắp xếp theo khối lượng nguyên tử trên một đường xoắn ốc quấn quanh hình trụ. Theo cách sắp xếp này, các nguyên tố có tính chất hóa học tương tự nằm trên cùng một đường sinh của hình trụ và cách nhau 16 đơn vị khối lượng nguyên tử. Tuy nhiên, ý tưởng này không thu hút được sự chú ý của các nhà khoa học đương thời.
Năm 1865, nhà hóa học người Anh John Alexander Newlands đưa ra “quy tắc bát âm”. Theo đó, ông nhận thấy sự lặp lại tính chất của các nguyên tố có thể so sánh với sự lặp lại các nốt nhạc sau mỗi 8 nguyên tố. Tuy nhiên, ý tưởng này không được giới khoa học thời đó chấp nhận và thậm chí còn bị chế giễu.
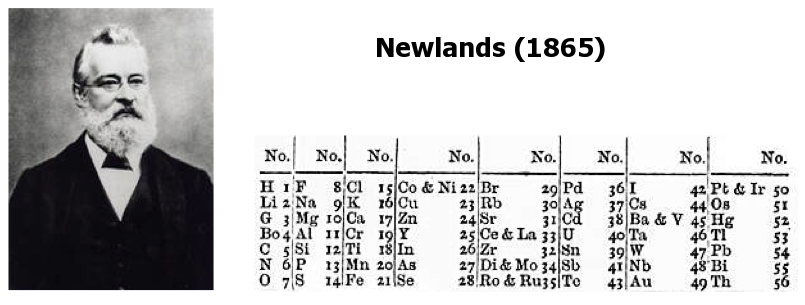
Trong bảng của Newlands (1865) các nguyên tố có tính chất tương tự nhau (mỗi nguyên tố có 1 số thứ tự), cũng như tương tự âm nốt nhạc trong bát âm được lặp lại sau 8 nguyên tố.
Năm 1864, nhà hóa học người Đức Julius Lothar Meyer công bố bảng gồm 27 nguyên tố được sắp xếp theo thứ tự tăng dần của khối lượng nguyên tử. Tuy nhiên, ông chưa rút ra được kết luận tổng quát nào. Đến năm 1870, Meyer công bố một hệ thống hoàn chỉnh hơn, trong đó thể hiện mối quan hệ giữa thể tích nguyên tử và khối lượng nguyên tử (đường cong Meyer).

Năm 1870 Meyer đã công bố bản sắp xếp đầy đủ các nguyên tố theo chiều tăng dần của trọng lượng nguyên tử và chỉ ra rằng qui luật tính chất của các nguyên tố là một hàm trọng lượng nguyên tử.
2. Định luật tuần hoàn
Mối quan hệ nào giữa các tính chất hóa học của hợp chất vô cơ và định luật tuần hoàn?
Định luật tuần hoàn được phát minh bởi nhà hóa học người Nga Dmitri Ivanovich Mendeleev vào năm 1869 trong quá trình ông biên soạn cuốn “Cơ sở hóa học”. Vào thời điểm đó, khoảng 63 nguyên tố đã được biết đến. Mendeleev gặp khó khăn trong việc hệ thống hóa các dữ liệu thực nghiệm về các nguyên tố và hợp chất của chúng. Dần dần, ông đi đến kết luận rằng tồn tại mối liên hệ giữa tính chất và khối lượng nguyên tử của các nguyên tố.
Bước đầu tiên là việc xây dựng “hệ thống thực nghiệm các nguyên tố” dựa trên khối lượng nguyên tử và sự tương đồng về tính chất hóa học. Khi lập bảng, Mendeleev đã tránh được sai lầm của Newlands, người cho rằng mỗi dãy phải có cùng số nguyên tố. Ông thiết lập các chu kì có độ dài khác nhau và để lại những chỗ trống cho các nguyên tố chưa được phát hiện, giải thích rằng chúng vẫn tồn tại nhưng chưa được tìm ra.

Trong bảng “Kinh nghiệm hệ thống các nguyên tố, được thiết lập dựa trên cơ sở trọng lượng nguyên tử và ái lực hóa học” (1869) Mendeleev đã sắp xếp các nguyên tố có cùng tính chất vào cùng một dãy.
Sau đó, ông phát biểu định luật: “Tính chất của các nguyên tố, cũng như tính chất của các đơn chất và hợp chất do chúng tạo thành, biến đổi tuần hoàn theo khối lượng nguyên tử của chúng”. Trong một số trường hợp, ông đặt nguyên tố có khối lượng nguyên tử lớn hơn trước nguyên tố có khối lượng nhỏ hơn, vì cho rằng số liệu khi đó chưa chính xác.
Trước đây, khái niệm “trọng lượng” thường được đồng nhất với “khối lượng”, nhưng ngày nay trọng lượng chỉ còn được hiểu là lực hấp dẫn tác dụng lên vật. Vì vậy, khái niệm “trọng lượng nguyên tử” được thay thế bằng “khối lượng nguyên tử”. Một số ngoại lệ trong thứ tự tăng dần khối lượng nguyên tử trong bảng tuần hoàn hiện đại được giải thích bằng sự tồn tại của các đồng vị.
Định luật tuần hoàn không có biểu thức toán học dưới dạng công thức, mà được thể hiện dưới dạng bảng – bảng hệ thống tuần hoàn các nguyên tố hóa học. Trong lịch sử, đã có hơn 50 dạng bảng tuần hoàn khác nhau được công bố, nhưng phổ biến nhất hiện nay là dạng bảng ngắn và bảng dài của Mendeleev.